世界保健機関(WHO)の2022年報告によると、2021年、マラリア常在国84カ国についての調査で2億4700万人がマラリアに感染し、62万人が死亡したと推定されている。マラリアでの死亡の96%は29カ国で、そのうち、ナイジェリア、コンゴ共和国、ニジェール、タンザニア共和国が半数以上を占めている(1)。
マラリアワクチンの開発は半世紀以上前から始まっていたが、2021年に重症マラリアを約30%減少させるワクチンが初めて承認され、接種が始まった。さらにWHOが目標とした70%の有効性を超すワクチンも開発され、第3相臨床試験の成績が近く発表されることになっている。マラリア対策の重要な節目になることが期待されている。
ワクチンの標的が定まる
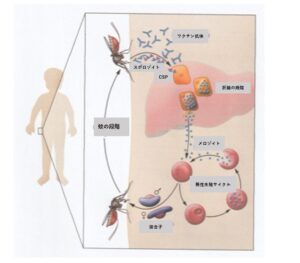
マラリアは、雌のハマダラカが吸血する際に唾液中に含まれるマラリア原虫のスポロゾイトが体内に侵入することで引き起こされる。スポロゾイトは肝臓に感染してシゾントに成熟し、メロゾイトとなって肝臓から放出されて赤血球に感染する。赤血球の中で無性生殖し、一部が接合子に分化して、カが吸血した際にカに摂取され、カの体内でふたたびスポロゾイトへと分化してヒトへの感染源となる。
1967年、米国ニューヨーク大学のルース・ヌッセンツヴァイクらは、マラリア原虫を摂取したハマダラカの唾液腺からスポロゾイトを集めて、X線で照射してマウスへの免疫を試み、マラリア感染を防げることを報告した。これがきっかけとなって、スポロゾイトの表面タンパク質(CSP: circumsporozoite protein)を標的としたワクチン開発が始まった(2)。
最初に承認されたRTS,Sワクチン
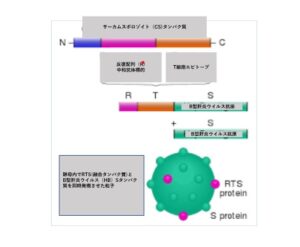
1996年には、グラクソ・スミス・クライン社がRTS、Sワクチン(商品名モスキリックス)を開発した。このワクチンは、図に示すように、CSPの反復配列(R)、T細胞エピトープ、B型肝炎ウイルスの表面タンパク質(S)を融合させたタンパク質を酵母で産生させたもので、B型肝炎ウイルスのような粒子となっている。それに免疫反応を増強するためにB型肝炎ウイルスSタンパク質が加えられている(3)。
なお、B型肝炎ウイルスのSタンパク質は、ウイルス粒子の殻(カプシド)を構成するもので、酵母で発現させると自然にウイルス粒子の形で産生されるので、ウイルス様粒子(VLP: virus like particle)ワクチンの基盤技術として多くのワクチン開発に利用されている。
2009年から2011年にかけてアフリカで、8922人の幼児と6537人の乳児で第3相臨床試験が行われた。その結果、幼児で約46%、乳児で約27%の有効性が見られた。接種は3回行い、免疫をさらに1,2年持続させるためには追加接種が必要と判断された(4)。
WHOが目指している75%の有効性には達していなかったが、4回接種グループでは死亡率が非常に低下し、重症マラリアでの入院がかなり抑えられていた。これらの成績からこのワクチンを却下するのはワクチン開発を大きく後退させると考えられたため、小規模のプロジェクトで4回の定期接種の可能性や死亡率への効果を調べることが提案された(5)。
2019年には、マラウイ、ガーナ、ケニアで83万人の小児へのワクチン接種が行われた結果、重症マラリアによる入院が約30%減少したことが認められた。そこで、2021年、WHOは中等度から高度流行地域での小児用としてワクチンを推奨した。それを受けて、ガーナ、続いてナイジェリアが承認した(6)。
2023年4月の時点で、ガーナ、ケニア、マラウイで150万人の子どもが定期接種計画に沿って少なくとも1回接種を受けている。
R21/マトリックスMワクチン
オックスフォード大学ジェンナー研究所はR21/マトリックスMワクチンを開発した。この研究所は新型コロナウイルスに対するアストラゼネカ・オックスフォードワクチンを開発したところである。R21/マトリックスMワクチンも、CSPとB型肝炎ウイルス Sタンパク質の融合タンパク質を酵母で発現させたVLPワクチンであるが、これに免疫反応を増強させるためのアジュバントとして、ノヴァヴァックス社のサポニン由来のマトリックスMが加えられている。
2022年12月、ブルキナファソで行われた臨床試験第2相の成績が発表された。3回の接種と追加接種から12ヶ月後におけるワクチンの有効性は高用量のアジュバント添加ワクチンで80%、低用量のアジュバントの場合で78%であった。これはWHOが目標としている75%を越えている(7)。
ガーナの食品医薬品局(FDA)はこのワクチンのガーナでの使用許可を与えた。第3相試験はブルキナファソ、ケニア、マリで4800人の子どもを対象として行われていて、その成績は今年末までに発表されることになっている。ジェンナー研究所のエイドリアン・ヒル所長はWHOにデータ提出後、1年以内に承認を得ることを目指している(8)。
文献
- World Health Organization: World malaria report 2022.
https://www.who.int/teams/global-malaria-programme/reports/world-malaria-report-2022
- Nussenzweig, R.S. et al.: Protective immunity produced by the injection of X-irradiated sporozoites of Plasmodium berghei. Nature, 216, 160-162, 1967.
- Stoute, J. A. et al. : A preliminary evalution of a recombinant circumsporozoite protein vaccine against Plasmodium falciparum New England Journal of Medicine, 336, 86-91, 1997.
- RTS,S Clinical Trials Partnership: Efficacy and safety of RTS,S/AS01 malaria vaccine with or without a booster dose in infants and children in Africa: final results of a phase 3, individually randomised, controlled trial. Lancet. 2015 July 04; 386(9988): 31–45.
- Greenwood, B., Doumbo, O.K.: Implementation of the malaria candidate vaccine RTS, S/AS01. Lancet, 387, 318-319, 2016.
- Zvala, F.: RTS,S: the first malaria vaccine. Journal of Clinical Investigation, 2022;132(1):e156588.
- Datoo, M.S. et al.: Efficacy and immunogenicity of R21/Matrix-M vaccine against clinical malaria after 2 years’ follow-up in children in Burkina Faso: a phase 1/2b randomised controlled trial. Lancet Infectious Diseases, 22, 1728-1736, 2022.
- University of Oxford: R21/Matrix-M™ malaria vaccine developed by University of Oxford receives regulatory clearance for use in Ghana. 13 April, 2023.
https://www.ox.ac.uk/news/2023-04-13-r21matrix-m-malaria-vaccine-developed-university-oxford-receives-regulatory