世界人口の半数以上が感染リスクにさらされているデングウイルス
日本で約70年ぶりに国内でのデングウイルスの感染者が3名見つかり、感染源の蚊が生息すると考えられた代々木公園で殺虫剤を散布する様子など、マスコミの報道が続いている。
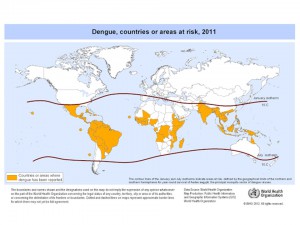
日本ではこれまでほとんど話題にならなかったデングウイルスだが、現在、中南米、東南アジア、西太平洋地域の120カ国に常在し、全世界の人口の半数以上の36億人が感染リスクにさらされている重要なウイルスである(図1)。
2013年には国際研究チームが、1960年から2012年にかけて世界各地で起きた8309回の発生のデータを解析した結果、年間3億9000万人が感染し9600万人が発病しているという推定をNatureに発表している1。国際交流の増加、温暖化による媒介蚊(ネッタイシマカ、ヒトスジシマカ)の生息域の拡大などのため、アフリカ、中近東、南アジアなどにも発生が広がってきている。ヒトスジシマカが生息する日本でも、以前から発生の可能性が指摘されていた。それが現実になったのである。
デングウイルスの発見と分離
臨床的にはデング熱の存在は古くから知られており、1779年にはバタヴィア(現在のジャカルタ)とカイロで同時に流行が記録されている。デング(dengue)は、スペイン語の「淑女気取り」を意味する言葉で、関節の痛みで足を曲げられない歩き方を指しており、スワヒリ語で痙攣を意味するディンガ(dinga)に由来すると考えられている。
デング熱がウイルスによる感染症ということは、1907年に明らかにされた。最初の動物ウイルスとして口蹄疫ウイルスが発見されてから8年目という早い時期だった。19世紀末から米国はフィリピンを実質的に植民地化したが、そこに駐留していた米軍兵士の間でデング熱の発生が起こり、大きな問題となった。軍医総監の命令により軍医のパーシー・アッシュバーン(Percy Ashburn)とチャールズ・クレイグ(Charles Craig)が原因解明にあたり、患者の血液を希釈し細菌フィルターを通過させたのち、志願した基地の兵士に接種して発病を確認し、濾過性ウイルスが原因ということを証明したのである。
しかし、デングウイルスが分離されたのは、35年後の第二次世界大戦のさなかの日本である。当時、京都帝国大学医学部微生物学教室に在籍していた堀田進博士(のちに神戸大学医学部教授)により行われたのである(図2;ご子息の堀田博・神戸大学教授提供)。私の手許に「Dengue and Related Arboviruses 」(デングおよび関連アルボウイルス*)という分厚い書籍がある。親しくお付き合いさせていただいた堀田博士から1995年にいただいたもので、博士の半世紀以上にわたるデングウイルス分野の研究論文をまとめたものである。これを参考にして、分離の経緯を簡単にまとめてみる。
*アルボウイルスは節足動物媒介ウイルスの意味で、昔の分類名。現在、デングウイルスはフラビウイルス科に分類されている。
1942年7月下旬、長崎・佐世保地域で突然デング熱が発生し、大阪、神戸にも広がった。南方の戦地からの船が持ち込んだものである。3ヶ月後には終息したが、翌年から1945年にかけて毎年発生し、広島、呉、福岡でも発生した。これらはすべて北緯33〜35度に位置していた。典型的な症状を示した患者の数は20万人とされたが、実際にはもっと多かったと考えられている。この大流行になった原因として、当時空襲に備えて置いてあった防火用水槽が蚊の増殖をもたらしたことが推測された。
この発生は熱帯病研究の貴重な機会となったため、堀田博士は長崎に調査に出かけた。発熱してから48時間以内の患者の血液を哺乳マウスの脳内に接種することによりマウスが衰弱し麻痺などを起こすことを確認した。望月という名前の44歳の女性の血液から分離したウイルスをマウスで継代したのち、志願者への接種実験を行いデング熱の症状が出ることを確かめた。これは望月株と名付けられ、世界で最初に分離されたデングウイルス株となった。1943年に日本語の論文でウイルス分離が報告され、英文論文が1952年Journal of Infectious Diseasesに発表された2。
1945年にはアルバート・セービン(Albert Sabin)*とウォルター・シュレジンガー(Walter Schlesinger)がハワイとニューギニアでウイルスを分離した。デングウイルスは患者の血清との反応の特徴から4つの血清型に分けられ、望月株ウイルスとハワイのウイルスは1型、ニューギニアのウイルスは2型に分類されている。3型と4型のウイルスは1956年にフィリピンでウイリアム・ハモンド(William Hammond)により分離された。
*のちに、生ポリオワクチンの開発者として有名になる。
デングワクチンの現状
デングウイルス感染では、一般に最初の感染では一過性で比較的軽くすむ場合が多い。そののち別の血清型のデングウイルスに再感染すると、デング出血熱やデング・ショック症候群という死にいたることもある重い症状をひき起こす。再感染は、最初のウイルス感染で産生された抗体が防御ではなく、むしろ症状を増悪させていると推測されている。そのため、すべての型のウイルスに効果のあるワクチンが求められる。普通のワクチンとは異なり、ワクチン接種がかえって重症化させるかもしれないのである。
このような難しい問題があったため、1945年、セービンがマウス脳を継代して作出した弱毒ワクチンを初めとして、多くの候補ワクチンが開発されてきたが、実用化に結びつくワクチンは出来てこなかった。
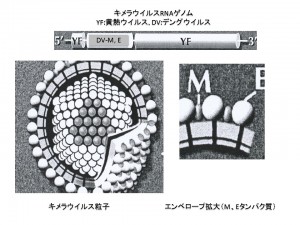
最近になって、やっと期待できるワクチンが現れてきた。フランスのサノフィ・パスツール社が開発したデング・黄熱キメラワクチンである。黄熱ウイルスとデングウイルスは同じフラビウイルス科に属しているRNAウイルスで、遺伝子構造が良く似ている。キメラワクチンは、図3に示したように、感染防御に働くと考えられるデングウイルスのエンベロープタンパク質(Eタンパク質とMタンパク質)の遺伝子を、黄熱ウイルスのそれぞれの遺伝子と置き換えたものである。この方法で1型から4型までのデングウイルスの遺伝子を持ったキメラワクチンが構築された。なお、デングウイルスの遺伝子が組み込まれたため、キメラウイルスはマウスやサルの脳内に接種してみると、元の黄熱ワクチンよりも弱毒になっている3。
4種類のキメラワクチンを混合したもの(4価デング・黄熱キメラワクチン)についての第2b相臨床試験がタイの4歳から11歳の小学生4000名で行われた。ワクチンは、1型に対しては約50%、3型と4型に対しては80~90%の防御効果が見られた。問題になったのは、2型で中和抗体は上がっていたのに、防御効果が9%と低かったことである4。
第3相臨床試験は、アジア地域(インドネシア、マレーシア、フィリピン、タイ、ベトナム)で10275人を対象として行われ、その結果が2014年7月Lancetに発表された。防御効果は、1型に対して50%、2型に対して35%、3型に対して78%、4型に対して75%という結果で、第2b相臨床試験よりも良い結果になっている。WHOでは期待できる成績とみなして、2014年中に出る予定のラテンアメリカにおける約2万人を対象とした試験の成績を待っている5。
文献
1. Bhatt, S., Gething, P.W., Brady, O.J. et al.: The global distribution and burden of dengue. Nature, 496, 504-507, 2013.
2. Hotta, S.: Experimental studies on dengue. I. Isolation, identification and modification of the virus. J. Infect. Dis., 90, 1-9, 1951.
3. 山内一也、三瀬勝利:ワクチン学。岩波書店、2014.
4.Sabchareon、A., Wallace, D., Sirivichayakul, C. et al.: Protective efficacy of the recombinant, live-attenuated, CYD tetravalent dengue vaccine in Thai schoolchildren: a randomized, controlled phase 2b trial. Lancet, 380, 1559-1567, 2012.
5. Capeding, M.R., Tran, N.H., Hadinegoro, S.R. et al.: Clinical efficacy and safety of a novel tetravalent dengue vaccine in healthy children in Asia: a phase 3, randomized, observer-masked, placebo-controlled trial. Lancet, Published Online July 11, 2014 http://dx.doi.org/10.1016/S0140-6736(14)61060-6