RSウイルスとは
RSウイルスは1956年、米陸軍ウォルターリード研究所で飼育されていたチンパンジーの間で鼻風邪の流行が起きた際、アンソニー・モリスたちにより細胞培養で分離された。最初、チンパンジーのウイルスと考えられたが、その翌年、ジョンスホプキンス大学のロバート・チャノックたちが肺炎や急性喉頭炎の幼児から同じウイルスを分離したことから、ヒトのウイルスがチンパンジーに感染したものと推測された。このウイルスは、感染した細胞で多核融合細胞(シンシチウム)*と呼ばれる変化を引き起こすことから、respiratory syncytial(呼吸器合胞体)ウイルスと名付けられた。一般には省略してRSウイルスと呼ばれている。
*(細胞の中に核は1個存在するが、多核融合細胞では細胞膜が融合して大きなひとつの細胞になっているため、複数の核が見つかる。)
ほとんどの人は2歳までに感染し、生涯を通して再感染を繰り返している。健康人では咳、頭痛、喉の痛みなど風邪の症状で済むが、65歳以上の高齢者、慢性の心臓や肺の疾患、または免疫能力の低下のある人では、肺炎など、重症化することがある。
2010年、WHOとビル&メリンダ・ゲイツ財団の資金援助でRSウイルス感染の世界的実態調査が行われた。ランセット誌に発表された報告によると、2005年に5歳未満の小児でRSウイルス感染による急性の下気道感染は3300万人を超え、そのうち少なくとも300万人以上が入院を必要とするものと推定された。この年にRSウイルス感染で死亡した5歳未満の小児は6万6000人から19万9000人で、その99%は発展途上国だった。世界的に重要な小児疾患ということがあらためて認識されたのである。
初期のワクチン
1960年代半ばには、ホルマリン不活化ワクチンが開発されたが、1967年、ワクチン接種を受けた小児2人がRSウイルス自然感染後に死亡する事例が起きた。ワクチン被接種者での重症化が問題になり、不活化ワクチンの接種は中止された。弱毒ワクチンが開発されたが効果が低く、RSワクチンの開発は半世紀の間、中断された。
RSウイルスワクチン開発の基盤となったブレークスルー
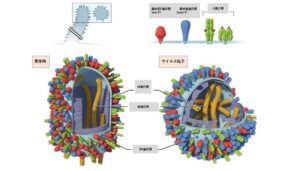
RSウイルスには11のタンパク質が含まれていて、ウイルス粒子表面に存在する2つの糖タンパク質(Gタンパク質とFタンパク質)が中和抗体を誘導する。ウイルスは、Gタンパク質が細胞膜の受容体に結合し、Fタンパク質を介して細胞膜に融合して細胞内に侵入する。
2000年、電子顕微鏡でFタンパク質に2つの異なる形態が存在することが見いだされた。2011年には、米国衛生研究所(NIH)ワクチン研究センターのグループと製薬企業ノバルティス社が、それぞれX線結晶解析により、RSウイルスのFタンパク質の原子レベルでの構造を明らかにした。それによると、細胞に融合する前のFタンパク質(pre F)蛋白は棒の先のキャンディーのような形をしている。細胞と融合したFタンパク質(post F)では構造が変化して、車のクラッチのような形になっている。(図1)
この発見に引き続いて、スペインのグループは、pre Fタンパク質に対する抗体が中和活性の大部分を占めていることを明らかにして、ワクチンの標的としてpre Fタンパク質が重要なことを示唆した。
2013年、NIHグループは、強い中和活性のある抗体が結合するFタンパク質の部位の分子構造をX線結晶解析により明らかにした。この部位はpre Fタンパク質に存在していたが、細胞膜に融合した後は消失していた。pre Fタンパク質の分子構造を修飾して安定化させてサルに接種したところ、post Fタンパク質接種の場合よりも70~80倍高い中和抗体が産生された。その結果、pre Fタンパク質がワクチン候補として取り上げられたのである。
この構造生物学によるRSウイルスワクチンの設計は、サイエンス誌による2013年の10大ブレークスルーのひとつに選ばれた。
1960年代に不活化ワクチンにより症状が増悪した原因は、不活化ワクチンではFタンパク質の立体構造がホルマリン処理により不安定になり、中和抗体が十分に産生されていなかったためと推測されている。
RSウイルスワクチンの開発レース
RSワクチンは高齢者用と妊娠女性用が開発の対象になっている。高齢者では加齢に伴う免疫力の低下などでRSウイルスに感染した場合重症化しやすい。とくに慢性閉塞性肺疾患(COPD)、喘息、慢性心不全の人では病態が悪化するおそれがある。米国では毎年、RSウイルスによる65歳以上の成人の入院が約17万7000例、死亡が1万4000例起きていると推定されている。日本の60歳以上の成人では、年間、約6万3000例の入院と4000例の死亡がRSウイルス感染によると推定されている。一方、妊娠女性用ワクチンは、母親からの移行抗体による乳幼児の感染防止(母子免疫)を目的としている。
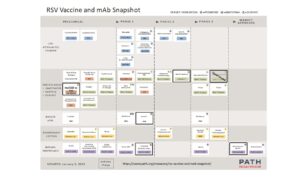
グローバル非営利健康組織PATHが2023年1月3日の時点における世界各国でのRSウイルスワクチンの開発状況をまとめている。第3相臨床試験に進んでいるのは、グラクソ・スミスクライン社(GSK)のサブユニットワクチン(高齢者用)、ファイザー社のサブユニットワクチン(妊娠女性用と高齢者用)、モデルナ社のRNAワクチン(高齢者用)、ババリアン・ノルディック社のMVAワクチニアウイルスを用いたベクターワクチン(高齢者用)、ヤンセン社のヒトアデノウイルス26型を用いたベクターワクチン(高齢者用)がある。GSK社の妊娠女性用ワクチンは、2022年2月に試験が中断された。(図2)
これらのワクチンのうち、GSKの高齢者用サブユニット(pre F)ワクチンは重症化を94%低下させることが確認され、2023年5月に、米国食品医薬品局(FDA)から初めて承認された。このワクチンは、チャイニーズハムスターの卵巣由来のCHO細胞で産生したpre Fタンパク質サブユニットワクチンである。ファイザー社の高齢者用サブユニット(pre F)ワクチンも5月末の承認が期待されている。
ファイザー社の妊娠女性用サブユニット(pre F)ワクチンは、臨床試験で生後90日以下の乳幼児でRSウイルス感染での重症化を82%防止したことが、2023年4月に発表された。このワクチンは、現在FDAで検討が行われていて、8月に結果が発表される予定になっている。
文献
山内一也、三瀬勝利:ワクチン学. 岩波書店、2014.
Abbasi, J.: RSV vaccines, finally within reach, could prevent tens of thousands of yearly deaths. Journal of American Medical Association, 327, 204-206, 2022.
McLellan, J.S., Ray, W.C. & Peeples, M.E. : Structure and function of RSV surface glycoproteins. Current Topics in Microbiology and Immunology, 372, 83-104, 2013.
Graham, B.S., Modjarrd, K. & McLellan, J. S.: Novel antigens for RSV vaccines. Current Opinion in Immunology, 35, 30-38, 2015.
白戸憲也:RSウイルスワクチン開発の現状(2022年)。IASR, 43, 94-95, 2022.
Valero, M.V.: ‘A good day’: FDA approves world’s first RSV vaccine. Nature, 03 May 2023.