ウイルス感染における免疫系の攻撃標的は、ウイルスとウイルス感染細胞である。中和抗体は、ウイルスに結合して感染性を失わせるため、防御の主役とみなされているが、抗体は細胞内には入り込めないため、感染した細胞内でのウイルス増殖を抑えることはできない。ウイルス感染での防御機構の全体像は、1980年代初め頃までは、主に動物実験で盛んに研究されていたが、ウイルス学が遺伝子レベルの研究に関心が移ってからは、研究されることはほとんどなかった。(1)
新型コロナウイルスの出現で、ウイルス感染における防御機構への関心は急速に高まってきた。患者での臨床面での知見が集まり、ワクチン接種による予防効果についてのデータが蓄積してきたことで、ヒトでの防御機構についての研究が進んできているのである。その状況を眺めてみる。
中和抗体とキラーT細胞
新型コロナウイルスの細胞への感染は、ウイルス粒子表面のスパイク(S)タンパク質の受容体結合領域(RBD)が、細胞表面に存在するウイルス受容体(ACE2)に結合することで始まる。Sタンパク質は1273個のアミノ酸から構成されていて、RBDは319番から514番のアミノ酸から成っている。中和抗体はこのRBDに対するものである。
新型コロナウイルス感染細胞の表面には、Sタンパク質だけでなく、細胞内で分解されたSタンパク質のペプチド(通常、5-8個のアミノ酸の配列)が、細胞膜の糖タンパク質である主要組織適合抗原(MHC)と複合体になって出現する。これはT細胞エピトープ(抗原決定基)と呼ばれ、キラーT細胞の増殖を誘導する。
ファイザーやモデルナの新型コロナワクチンは、Sタンパク質のメッセンジャー(m)RNAを脂質のナノ粒子に包み込んだもので、筋肉内に注射される。筋肉細胞内では、mRNAの情報に従ってSタンパク質が合成され、細胞表面に出現し、B細胞により中和抗体が産生される。一方、細胞表面にはT細胞エピトープも出現してキラーT細胞の増殖を誘導する。すなわち、mRNAワクチンは抗体産生とキラーT細胞の誘導を引き起こすのである。なお、アストラゼネカのベクター・ワクチンも同様に、抗体産生とT細胞の増殖を誘導する。(2)
米国アレルギー感染症研究所のグループは、2019年に新型コロナウイルス感染から回復した30名について、キラーT細胞のエピトープを解析した。当時は、英国のアルファ株、南アフリカのベータ株、ブラジルのガンマ株が流行していて、デルタ株はまだ出現していなかった。新型コロナウイルスのSタンパク質の1300近いアミノ酸配列からT細胞のエピトープになると考えられた52種類のアミノ酸配列では、3つの変異株の間で、1カ所を除いて、すべて保存されていた。デルタ株で問題になっているのは、中和抗体の標的となるRBD結合領域の変異であり、キラーT細胞のエピトープは変異を起こさず保存されていることが推測された。 (3)
新型コロナウイルス患者でのキラーT細胞の関与については、シンガポールのDuke-NUS Academic Medical Centerグループが、発病後15日以内の早期にキラーT細胞の数が上昇するという論文を発表している。 (4)
mRNAワクチンでは、ドイツのフライブルグ大学のグループが、ファイザー・ワクチンの臨床試験で、1回接種後10〜12日目の中和抗体が出現していない時期から、防御効果が見られたことに注目して、キラーT細胞の検出を試みている。その結果、ワクチン接種1週間後には、キラーT細胞が動員されていることを見いだし、中和抗体などの免疫が成立する前からキラーT細胞が防御に働くことを主張している。 (5)
イタリアなどで、X連鎖無ガンマグロブリン血症という遺伝疾患の患者が新型コロナウイルス感染から回復したことが報告されている。これらの患者は抗体を産生できないので、キラーT細胞による防御の重要性を示唆するものとみなされている。 (6)
抗体依存細胞媒介細胞傷害(ADCC)
感染細胞の破壊機構として、キラーT細胞とは別に、抗体依存細胞媒介細胞傷害(ADCC)という仕組みがある。ウイルス感染細胞の表面には早い時期からウイルス抗原が出現する。抗体には可変領域(抗原が結合する部位)と定常領域(Fc)があって、感染細胞に結合した抗体のFcに対し、Fc受容体を持つリンパ系細胞が攻撃して、感染細胞を破壊する ADCCと呼ばれる仕組みがある。Fc受容体を持つリンパ系細胞には、NK細胞、マクロファージや好中球などがあるが、主にNK細胞がエフェクター細胞として細胞を攻撃すると考えられている。図に示すように、NK細胞内にはグランザイムとパーフォリンを含む細胞毒性顆粒があって、Fcを介して感染細胞に結合すると、この顆粒が注入されて細胞死(アポトーシス)をもたらすと説明されている。(図)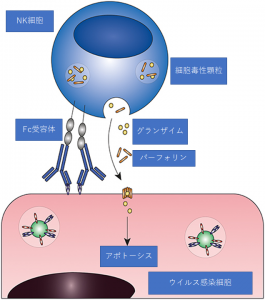
ADCCは、小児に肺炎を起こすRSウイルス、インフルエンザウイルス、ヒト免疫不全ウイルス(HIV)などで、とくに注目されている。コロナウイルスでは、風邪コロナウイルス229Eについて、培養細胞でADCCが報告されている。(7)
米国ネブラスカ大学リンカーン校のグループは、新型コロナ患者の血液に、エフェクター細胞として、Fc受容体を発現させたNK細胞(リンパ腫の患者のリンパ球から樹立した細胞株)を加えて、新型コロナウイルス感染細胞に対する破壊効果を調べた。その結果、中和抗体と非中和抗体ともにADCC活性を示すことが見いだされた。(8)
シンガポールのDuke-NUS Academic Medical Centerグループは、20人の医療従事者でファイザーのmRNAワクチンを1回接種後のSタンパク質に対する抗体とT細胞の産生を調べたところ、7日目には抗体は検出されなかったが、10日目には中和活性のない抗体が検出された。一方、血液中には、顆粒を放出したNK細胞の上昇が見いだされた。NK細胞の活性化が推測されることから、この早期の抗体は、ADCCを介して防御に働いている可能性が推測された。なお、キラーT細胞の出現も確認されている。(9)
まとめ
ヒトの身体に備わっているウイルスに対する防御の担い手は中和抗体だけではない。しかし、中和抗体以外の担い手は、検出が難しく、定性的に調べなければならないため、定量的に測定できる中和抗体がワクチンの防御効果を推測する指標の役割を受け持っているのである。
ここで取り上げた機構のほかに、補体媒介細胞傷害(CDC)がある。補体とは血液中に存在する一群のタンパク質で、抗体の働きを補う役目を受け持っている。CDCはウイルス感染細胞の表面に結合した抗体が補体を活性化して、細胞の溶解を引き起こすもので、重要な防御機構とみなされるが、適当な検出手法がないためか、新型コロナウイルス感染での報告は見当たらない。
文献
- 山内一也:ウイルス感染と免疫、中外医学社、1979
- Rijkers, G.T., Weterings, N., Obregon-Henao, A. et al.: Antigen presentation of mRNA-based and virus-vectored SARS-CoV-2 vaccines. Vaccines 2021, 9, 848. https:// doi.org/10.3390/vaccines9080848
- Redd, A.D., Nardin, A., Kared, H. et al.: CD8+ T-cell responses in COVID19 convalescent individuals target conserved epitopes from multiple prominent SARS-CoV-2 circulating variants. Open Forum Infectious Diseases. March 24, 2021. DOI: 10.1093/ofid/ofab143
- Oberhardt, V., Luxenburger, H., Kemming, J. et al.: Rapid and stable mobilization of CD8+ T cells by SARS-CoV-2 mRNA vaccine. Nature, 597, 268-273, 2021.
- Tan, A.T., Linster, M., Tan, C.W. et al.: Early induction of functional SARS-CoV-2-specific T cells associates with rapid viral clearance and mild disease in COVID-19 patients. Cell Reports 34, 108728, February 9, 2021.
- Soresina, A., Moratto, D., Chiarini, M. et al.: Two X-linked agammaglobulinemia patients develop pneumonia as COVID-19 manifestation but recover. Pediag. Allergy Immunol., 2020. 00: 1-5.
- Holmes, M.J., Callow, K.A., Childs, R.A. et al.: Antibody cellular cytotoxicity against coronavirus 229E-infected cells. British J. Exp. Pathol., 67, 581-586, 1986.
- Tso, F.Y., Lidenge, S.J., Poppe, L.K. et al. (2021) Presence of antibody-dependent cellular cytotoxicity (ADCC) against SARS-CoV-2 in COVID-19 plasma. PLoS ONE 16(3): e0247640. https://doi.org/10.1371/ journal.pone.0247640
- Kalimuddin, S., Tham, C.Y.L., Qui, M. et al.: Early T cell and binding antibody responses are associated with COVID-19 RNA vaccine efficacy onset. Med 2, 682-688, 2021.
