ジカウイルスに関わる問題や対策は、これまでに76回(地球温暖化で広がるジカウイルス:乳児の小頭症との関連が浮上)、79回(ジカウイルス感染に伴う小頭症とギラン・バレー症候群)、87回(ジカウイルスによる小頭症のサル・モデル)、98回(昆虫の共生細菌ボルバキアがジカウイルスなどの伝播を阻止する分子機構)で取り上げてきた。今回は米国の2つのグループが競い合っているジカウイルスDNAワクチンの開発の進展状況を紹介する。
ジカウイルス感染は半世紀以上前から散発していたが、2013年から2014年にかけてフランス領ポリネシアで2万人近い感染者が発生して注目された。この流行では、ジカウイルスが原因と考えられるギラン・バレー症候群(四肢の筋力の低下などを伴う急性神経炎)の患者42名が見いだされた。2015年には、ブラジルで爆発的な流行が起きた。この際に生まれた子どもに見られた小頭症がジカウイルスによることが明らかになり、全世界に衝撃を与えた。感染はその後、中南米、カリブ海地域、米国フロリダにも広がり、2016年2月に、WHOは公衆衛生における緊急事態と発表した。
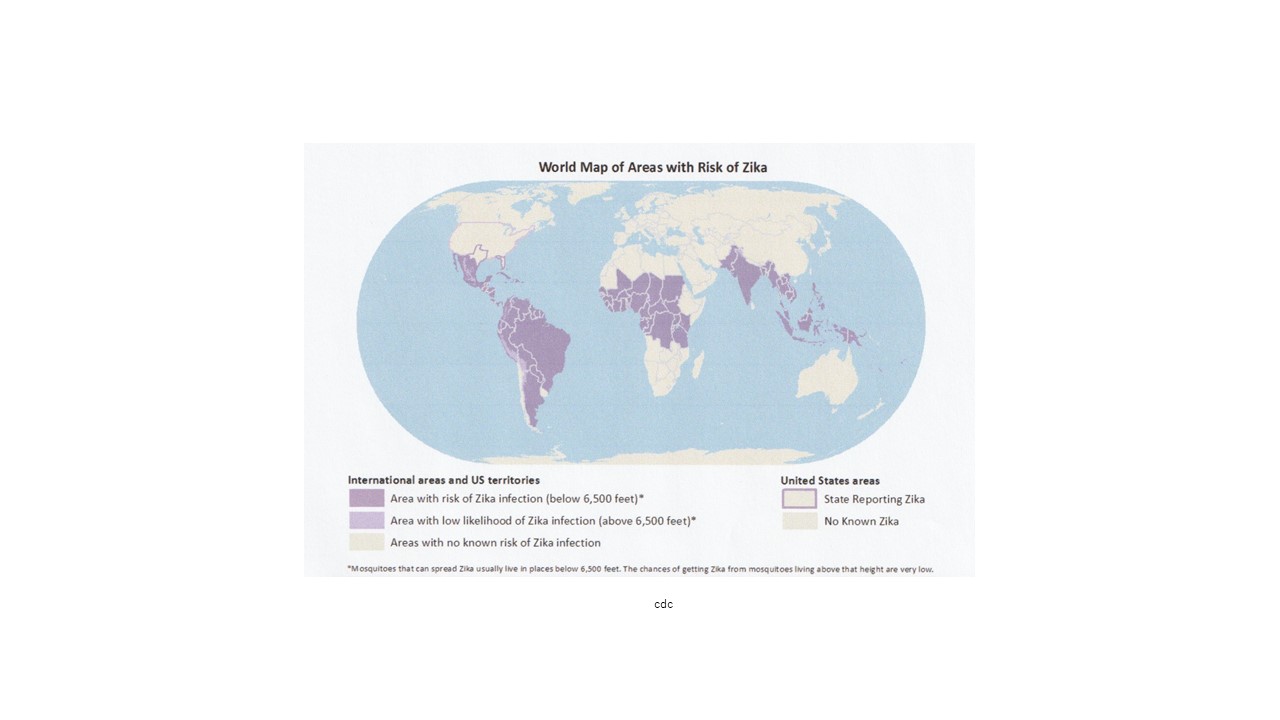
ジカウイルス感染のリスクを抱えた国は、図のように全世界に広がっている(2017年8月の時点)。健康な成人が感染した場合には、軽症または無症状に終わることが多いが、妊婦が感染した場合には先天性小頭症の子どもが生まれるおそれがある。そこで、ジカウイルス地域の住民、旅行者が持ち込んだ場合に、妊娠可能年齢の女性および、精液からの伝播を引き起こすおそれのある配偶者に接種するワクチンの開発が喫緊の課題になっている。
WHOの緊急声明から、わずか半年後には2つのジカウイルスDNAワクチンの臨床試験が始まった。国立衛生研究所(NIH)ワクチン研究センターのグループが開発したワクチン、もう一つは、ウイスター研究所とInovio Pharmaceuticalsが開発したワクチンである。
ジカウイルスは、フラビウイルス科に属している。同じ科にはウエストナイルウイルス、日本脳炎ウイルス、デングウイルスなどが含まれていて、これらのウイルスの増殖機構については次のような知見が蓄積されている。感染防御の中心は、ウイルスのエンベロープ内のEタンパク質に対する抗体で、抗体の標的となる領域もEタンパク質の立体構造の解析により明らかにされている。Eタンパク質では次のような産生様式が明らかにされている。まず細胞内でM(membrane)タンパク質の前駆体(precursor M: prM)とEタンパク質を含む未成熟粒子が産生される。Eタンパク質とprMタンパク質の遺伝子は隣接していて、両タンパク質が2量体となってEタンパク質が形成され、成熟ウイルスとなる。
NIHグループ、ウイスター研究所グループともに、この知見にもとづいて、Eタンパク質とprMタンパク質をコードするDNAワクチンを構築した。ワクチンの筋肉内注射により、細胞内でEタンパク質とprMタンパク質を発現させて、Eタンパク質粒子を形成させ、これにより免疫系を刺激するという戦略である。DNAワクチンの欠点は、免疫効果が弱いことだが、ウイルスと同様の粒子状にすることで、免疫効果を高めることをねらっている。こうして、ジカウイルスEタンパク質遺伝子とprM遺伝子をプラスミドDNAに組み込んだ2つのDNAワクチンが開発された。
NIHグループは、世界各地で分離されたジカウイルスが中和試験で単一の血清型であることから、フランス領ポリネシアで分離したウイルスのEタンパク質DNAとprMタンパク質DNAを分離してワクチンを構築した。最初、マウスに接種して中和抗体が上昇することを確かめた上で、18頭のアカゲザルの筋肉内に2回接種した。8週後にジカウイルスで攻撃したが、17頭(94%)のサルで血液中にジカウイルスは検出されず、感染が阻止されたことがうかがえた。デングワクチンなど、フラビウイルスのワクチンでは、免疫が不十分もしくは低下した場合に、自然感染での症状を逆に悪化させることがある。これは、抗体がウイルスの増殖阻止ではなく、促進するためである。しかし、サルでは、そのような促進抗体や、ウイルスの増殖促進はみられなかった。
動物実験の結果を受けて、2016年8月、第1相臨床試験がNIH病院など米国内の3カ所で、80人あまりのボランティアで始められた。2017年初めに安全性と抗体産生が確認され、3月末に第2/2b 相試験が始められた。対象は、ジカウイルス感染が確認された地域や蚊によるウイルス媒介の危険性のある地域で、米国、プエルトリコ、ブラジル、ペルー、コスタリカ、パナマ、メキシコで、約2500人にワクチンをジェット注射器(注射針を用いない)で筋肉内に接種し、安全性、抗体産生、最適ワクチン量の確認、そして、感染防止効果を調べることになっている。
ウイスター研究所グループは、1952年から2015年の間で分離されたジカウイルスのprM遺伝子とE遺伝子のうち保存されている配列にもとづいてワクチンを構築した。prMとEのデザインはNIHと若干異なるが、基本的な戦略は同じである。
最初の動物試験は、自然抵抗性を担うインターフェロンの受容体を破壊したマウスで行われた。このマウスはジカウイルスを接種すると、活動が鈍り神経症状を示して死亡する。しかし、ワクチン接種したマウスでは抗体が産生され、ジカウイルスで攻撃しても発病しなかった。次ぎに試験したアカゲザルでは、抗体と細胞性免疫が成立したことが確かめられた。
第1相臨床試験は、NIHとほぼ同じ時期の2016年8月から、米国とカナダで総計40名のボランティアに対して始められた。ワクチン接種は、NIHと異なり、エレクトロポレーションで行われた。その結果、安全性が確認され抗体が産生されたことが、2017年10月に報告された。
参考文献
山内一也:ウイルス・ルネッサンス。東京化学同人、2017.
Allison, S.L., Stadler, K., Mandl, C.W. et al.: Synthesis and secretion of recombinant tick-borne encephalitis virus protein E in soluble and particulate form. J. Virol. 69, 5816–5820 (1995).
Dowd, K.A., Ko, S.-Y., Morabito, K.M. et al.: Rapid development of a DNA vaccine for Zika virus. Science 10.1126/science.aai3197 (2016).
Muthumani, K., Griffin, B.D., Agarwal, S. et al.: In vivo protection against ZIKV infection and pathogenesis through passive antibody transfer and active immunisation with a prMEnv DNA vaccine. Npj Vaccines (2016) 1, 16021; doi:10.1038/npjvaccines.2016.21
Tebas, P., Roberts, C.C., Muthumani, K. et al. : Safety and immunogenicity of an anti–Zika virus DNA vaccine — Preliminary report. N. E. J. Med., 2017, Oct.
DOI: 10.1056/NEJMoa1708120